Belangrijke stap op weg naar genezing van sporadische ALS
17-10-2013
Experimentele gentherapie in een muismodel van sporadische ALS
Graduate School of Medicine
Amyotrofische Laterale Sclerose (ALS) ontwikkelt zich voornamelijk op middelbare leeftijd en ouder en wordt gekenmerkt door progressieve spierzwakte en musculaire atrofie. Er is geen behandeling voor deze ongeneeslijke neurologische ziekte die tot de dood leidt als gevolg van de verlamming van de ademhalingsspieren, en dit binnen een paar jaar. De onderzoeksgroep van project Professor Shin Kwak (visiting onderzoeker, klinisch laboratorium biotechnologie, Centrum voor pathobiologie en integratiegeneeskunde, Graduate School of Medicine, Universiteit van Tokio; Project Professor, Clinical Research Center voor geneeskunde, Internationale Universiteit voor gezondheid en welzijn) had in eerder onderzoek ontdekt dat het enzym ADAR2 betrokken was bij celdood van neuronen in niet-familiale ALS, die voorkomt in de grote meerderheid van de gevallen van de ziekte.
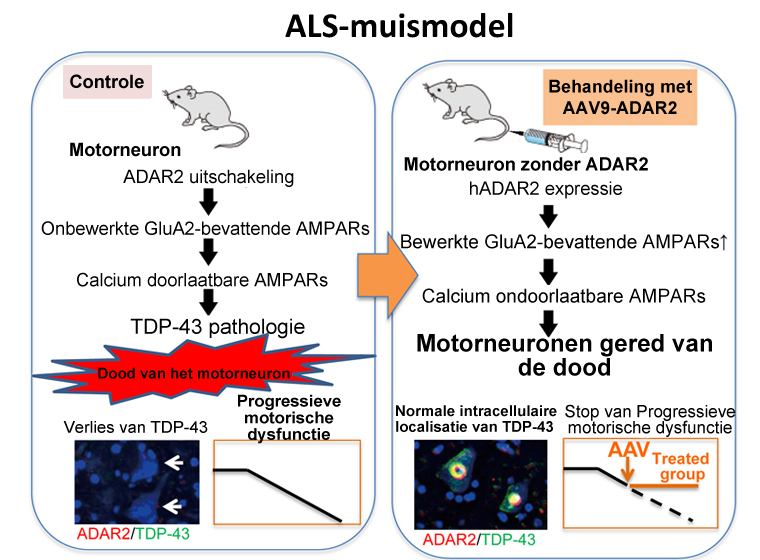
© team Kwak, een enkele intraveneuze injectie van de AAV9 vector leverde met succes het menselijke ADAR2 (RNA bewerkend enzym) gen aan motorische neuronen van AR2 muizen, waaruit het ADAR2 gen selectief was weggehaald uit de motor neuronen, om zo een mechanisch muismodel voor sporadische ALS te maken. De resulterende expressie van het ADAR2 voorkwam effectief de dood van motorneuronen in de AR2 muizen en progressieve motorische dysfunctie.
In deze studie hebben Project Professor Kwak en Project Onderzoeker Takenari Yamashita (klinisch biotechnologie laboratorium, Centrum voor pathobiologie en integratie geneeskunde, Graduate School of Medicine, Universiteit van Tokio), in samenwerking met de onderzoeksgroep van Special Professor Shinichi Muramatsu's (Jichi Medical University), een adeno-associated virus serotype 9 (AAV9) vector ontwikkeld waardoor gen toelevering alleen aan de neuronen van muis in de hersenen en het ruggenmerg toegestaan wordt. Nadat deze vector werd toegediend door intraveneuze injectie in de sporadische ALS-muizen (AR2), slaagden de onderzoekers er met succes in om voor de eerste keer de degeneratie en het verlies van motorische neuronen en de progressie van de symptomen van de ziekte te stoppen.
Bovendien, zelfs wanneer toegediend na het ontstaan van symptomen, leidde de expressie van het ADAR2 gen in motorische neuronen tot stopzetting van het proces dat leidt tot celdood en symptomen als gevolg van celdood werden zonder eventuele schijnbare neveneffecten voorkomen. Conventioneel denkt men dat het moeilijk is om genetisch materiaal in de hersenen en het ruggenmerg in te brengen door intraveneuze injectie, maar een enkele intraveneuze injectie was voldoende voor langdurige expressie van een effectieve hoeveelheid van het ADAR2 gen door het gebruik van de AAV9 vector om genexpressie alleen in neuronen te triggeren.
Hoewel dit resultaat in een muismodel werd bereikt, denkt men dat een soortgelijk moleculair mechanisme ten grondslag ligt aan sporadische ALS bij menselijke patiënten, en vermits het menselijk ADAR2 gen een therapeutisch effect had in het muismodel, wordt verwacht dat een soortgelijke vorm van gentherapie effectief zal zijn bij de behandeling van menselijke ALS. De AAV9 vector staat bovendien bekend als veilig, en na bevestiging van de veiligheid van de verbeterde AAV9 vector en het bepalen van de optimale dosering, is het te hopen dat dit onderzoek een nieuwe route naar de behandeling van ALS opent. Gentherapie heeft momenteel een sterk imago als een vervangende therapie voor zeldzame genetische aandoeningen, maar dit onderzoek is uniek omdat het toont dat gentherapie zelfs mogelijk is in sporadische gevallen als de moleculaire pathologie van de ziekte is doorgrond.
Dit onderzoek werd gepubliceerd in EMBO moleculaire geneeskunde (24 September 2013 online editie). De huidige studie werd uitgevoerd met de steun van het Japans wetenschap en technologie Agentschap voor strategische fundamentele onderzoeksprogramma's (CREST) en het ministerie van gezondheid, arbeid en welzijn voor middelen voor aan ziekte-gerelateerde handicaps Research Program.
Artikel: Takenari Yamashita, Hui Lin Chai, Sayaka Teramoto, Shoji Tsuji, Shimazaki Kuniko, Shin-ichi Muramatsu en Shin Kwak,
" "Redding van fenotype van Amyotrofische Laterale Sclerose in een muismodel na intraveneuze toelevering van AAV9 -ADAR2 aan motorneuronen." "
EMBO moleculaire geneeskunde Online editie: 2013/9/24 (Japan keer), doi: 10.1002/emmm.201302935.
Artikel - Klik hier
Vertaling: ALS Liga: Anne
Bron: The University of Tokyo
Gebruik van virus bij ALS-gentherapie
In een nieuw onderzoek dat is gepubliceerd in Human Molecular Genetics hebben Packard-wetenschapper Zuoshang Xu en collega’s van de universiteit van Massachusetts een stam van het recombinant adeno-associated virus (rAAV) ontdekt dat in de toekomst wellicht gebruikt kan worden bij gentherapie voor ALS-patiënten. De bevindingen zijn van groot belang, aldus Xu, omdat nu voor het eerst is aangetoond dat via een eenmalige intrathecale injectie van een bewerkt virus een ziektebestrijdend gen door het hele zenuwstelsel kan worden getransporteerd.
 Xu en zijn collega’s besloten het virus rechtstreeks te injecteren in de ruggenmergvloeistof dat het ruggenmerg en de hersenen omsluit. Naar hun overtuiging zou hierdoor met een enkele injectie het virus een groot gedeelte van het centrale zenuwstelsel kunnen bereiken. Er bestaan veel serotypen van rAAV, en Xu en zijn collega’s wilden erachter komen welk type het meest veelbelovend was voor toekomstige onderzoeken met mensen. In een nieuw artikel in Human Molecular Genetics beschrijven ze hoe ze vijf serotypen hebben getest bij muizen en dat twee daarvan (rAAV9 en rAAVrh10) cellen wisten binnen te dringen over de gehele lengte van het ruggenmerg. Om te weten te komen of dit ook bij mensen zou kunnen werken, hebben ze een volwassen zijdeaapje een enkele intrathecale injectie van rAAVrh10 toegediend, waarna ze constateerden dat het virus zich net zoals bij de muizen over de gehele lengte van het ruggenmerg verspreidde.
Xu en zijn collega’s besloten het virus rechtstreeks te injecteren in de ruggenmergvloeistof dat het ruggenmerg en de hersenen omsluit. Naar hun overtuiging zou hierdoor met een enkele injectie het virus een groot gedeelte van het centrale zenuwstelsel kunnen bereiken. Er bestaan veel serotypen van rAAV, en Xu en zijn collega’s wilden erachter komen welk type het meest veelbelovend was voor toekomstige onderzoeken met mensen. In een nieuw artikel in Human Molecular Genetics beschrijven ze hoe ze vijf serotypen hebben getest bij muizen en dat twee daarvan (rAAV9 en rAAVrh10) cellen wisten binnen te dringen over de gehele lengte van het ruggenmerg. Om te weten te komen of dit ook bij mensen zou kunnen werken, hebben ze een volwassen zijdeaapje een enkele intrathecale injectie van rAAVrh10 toegediend, waarna ze constateerden dat het virus zich net zoals bij de muizen over de gehele lengte van het ruggenmerg verspreidde.
Wat resteerde was de vraag of deze methode ook therapeutische effecten kon hebben bij ALS. De onderzoekers hebben daartoe een rAAVrh10 transportvirus ontwikkeld en vervaardigd dat een gen kan transporteren dat inwerkt op gemuteerd SOD1 mRNA en daarmee de productie van misvormd eiwit kan voorkomen. In een muismodel van ALS (waarbij de muizen drager waren van een menselijke SOD1-mutatie), hebben de onderzoekers het virus getest door middel van een enkele intrathecale injectie. Zij zagen vervolgens dat het virus de expressie van SOD1 onderdrukte en het ziekteverloop vertraagde.
“Het is opmerkelijk dat we al bij onze eerste poging een serotype vonden dat werkte,” aldus Xu. “Wellicht wordt AAV in de toekomst gebruikt om ALS te behandelen, waarbij waarschijnlijk slechts een klein aantal injecties nodig is.”
Bron: Packard Center


