La recherche aide à dépister les causes de la SLA
11-04-2014
Madison, Wisconsin (USA), 3 avril 2014
Un chercheur de l'Université du Wisconsin-Madison a découvert un défaut dans la formation des protéines lors de l’examen des cellules nerveuses de patients souffrant de maladies neurologiques graves. Ce défaut pourrait s’avérer être la clé du développement de la sclérose latérale amyotrophique (SLA).
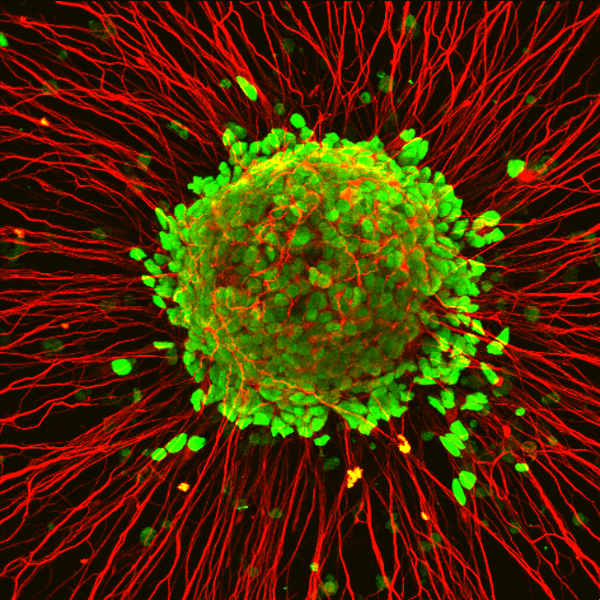
Photo : Dans cette image microscopique de motoneurones moteurs du laboratoire du Su-Chun Zhang, le noyau est colorié en vert et les fibres nerveuses en rouge. Zhang et son équipe du Waisman Center ont découvert que le dysfonctionnement d'une protéine du noyau de la cellule constituait probablement la première étape du processus de la maladie. (Image : Hong Chen, Su-Chun Zhang/Waisman Center).
La SLA provoque la paralysie et est mortelle. Selon l'ALS Association, environ 30.000 Américains souffrent de SLA.
Depuis la découverte d'une mutation génétique chez un petit groupe de patients SLA, les scientifiques l’ont inoculée chez des animaux de laboratoire afin de trouver un traitement pour la maladie. Cette approche n'a pas encore porté de fruits, selon Su-Chun Zhang, neuroscientifique au Waisman Center de UW-Madison. Il est aussi l'auteur principal d’un nouveau rapport, publié le 3 avril dans la revue Cell Stem Cell.
Zhang a utilisé une nouvelle méthode : il a examiné en laboratoire des cellules humaines malades. Ces cellules, appelées motoneurones, commandent les muscles et sont affectées par la SLA.
Zhang a été le premier au monde, il y a environ 10 ans, à réussir à produire à des motoneurones à partir de cellules souches embryonnaires humaines. Plus récemment, il a étendu cette méthode en changeant des cellules de peau en cellules souches pluripotentes induites (iPS), qui ont été, à leur tour, transformées en motoneurones.
Les cellules iPS sont utilisables en tant que « modèle de maladie » parce qu'elles possèdent les qualités du donneur. Selon Zhang, la méthode iPS a un avantage important par rapport à la méthode génétique « qui ne permet d’étudier qu’uniquement les effets d'un gène connu, induisant la maladie ». « Avec iPS, nous pouvons prélever les cellules des patients et les transformer en motoneurones. Cela nous permet d’observer d'une façon tout à fait différente la pathologie fondamentale de la maladie. »
Zhang, Hong Chen chercheur à Waisman et leurs collègues se focalisent, dans leur dernier rapport, sur les protéines responsables de la construction de la structure de transport au sein des motoneurones. Grâce à cette structure, appelée neurofilaments, des matériaux et des organes cellulaires sont transportés vers les extrémités de la cellule nerveuse. La charge transportée inclus des neurotransmetteurs, qui transmettent des signaux aux muscles, et des mitochondries, organites qui produisent de l'énergie.
Selon Zhang, les motoneurones qui contrôlent les mouvements des pieds ont des filaments d'environ un mètre de long, et les neurotransmetteurs doivent être acheminés du noyau cellulaire sur toute cette longueur vers le lieu d’où ils d'envoient le signal aux muscles. Le patient chez qui cette connexion échoue, devient paralysé. Les premiers symptômes de la SLA sont ainsi fréquemment situés dans les pieds et les jambes.
Les scientifiques savent depuis longtemps que la SLA provoque des blocages dans les filaments neuronaux. Ces blocages sont provoqués par un enchevêtrement de protéines déformées qui entrave le transport au sein de la ramification nerveuse. Cela mène finalement au dysfonctionnement et à la mort de la ramification nerveuse. On vient, maintenant, de découvrir la source de ces blocages : une carence de l'une des trois protéines qui composent les neurofilaments.
Selon Zhang, les filaments neuronaux ont un rôle structurel et fonctionnel. « Tout comme les connexions, les madriers et les murs porteurs d'une maison, les neurofilaments sont l'épine dorsale des cellules, mais ils changent constamment. Ces protéines doivent être transportées du noyau cellulaire, où elles sont produites, à l'extrémité éloignée de la cellule et ensuite rapportées pour être recyclées. Si les protéines ne se replient pas correctement, elles deviennent plus difficiles à transporter et forment un agrégat confus qui induit une série de problèmes. »
Zhang explique que, si ces agrégats de protéines avaient déjà été constatés chez des patients SLA, on ne savait pas comment, ni quand ou pourquoi ils se formaient. Maintenant que les chercheurs disposent de millions de cellules porteurs de forme humaine de la maladie, l’équipe de Zhang a découvert la cause de ces accumulations de protéines qui constituent les neurofilaments. Zhang déclare: « Nous avons constaté que la SLA est causée par une erreur dans l'une des étapes de la production des neurofilaments ».
Zhang ajoute que « des accumulations confuses semblables » peuvent aussi être constatés chez des patients atteints d’Alzheimer et de Parkinson. « La prise de conscience que nous pouvions, par cette recherche SLA, trouver aussi la cause de nombreuses autres maladies neurodégénératives était très excitante. »
Zhang ajoute au sujet de cette étude, effectuée par son équipe, sur des motoneurones cultivés à partir de cellules souches du patient: « Nous avons fait une découverte remarquable. Les motoneurones que nous avions reprogrammés à partir des cellules de la peau, étaient relativement jeunes et nous avons vu que la défectuosité de la protéine se produit dès le départ. Ce qui signifie que c'est la cause la plus probable de la maladie. Ce n'était pas encore connu, mais je pense que si nous parvenons à intervenir dans cette étape précoce du processus de la maladie, nous pourrions sauver la cellule nerveuse. »
Au cours de ses expériences, Zhang a trouvé un moyen de protéger, en laboratoire, les cellules nerveuses de la destruction. Selon Zhang, après que son équipe ait manipulé le gène qui a conduit à la formation de la protéine défectueuse « les cellules sont soudainement redevenues normales ».
Il ajoute que les scientifiques de « Small Molecule Screening and Synthesis Facility » de UW-Madison sont actuellement également à la recherche d'un moyen pour sauver les motoneurones malades. Ces neurones sont produits à partir des millions de cellules souches à l'aide de la technique que Zhang a perfectionnée au fil des années.
Zhang raconte : « Des bibliothèques entières de candidats-médicaments, chacune composée d'un millier ou plus de ces produits, sont actuellement à l'essai. C'est très excitant. Nous pouvons le faire maintenant. La recherche fondamentale commence maintenant à porter ses fruits. Avec une maladie comme la SLA, bien sûr, il n'y aucun temps à perdre. »
Traduction : Fabien
Source : University of Wisconsin-Madison
Lisez aussi: The origin of Lou Gehrig´s disease may have just been discovered et What Causes Lou Gehrig’s Disease? Scientists Believe They´ve Found The Answer


