Cytokinetics annonce résultats de FORTITUDE-ALS, essai clinique de phase 2 de Reldesemtiv chez des patients SLA a la réunion annuelle de l’Academie Neurologique Américaine
07-05-2019
L'essai n'a pas rencontré d'importance statistique pour l'analyse d'efficacité principale
Les patients sous toutes les doses de Reldesemtiv ont régresse moins que les patients sous placebo pour SVC et ALSFRS-R, avec des différences cliniquement significatives apparaissant au fil du temps
Résiliations précoces et événements indésirables graves ont été équilibrés pendant le traitement
SOUTH SAN FRANCISCO, Californie, Cytokinetics, Incorporated. Lors d’une podium présentation powerpoint à la réunion annuelle de l’American Academy of Neurology à Philadelphie,Jeremy Shefner, MD, Ph.D., chercheur principal de FORTITUDE-ALS, professeur et titulaire de la chaire de neurologie au Barrow Neurological Institute, et professeur et titulaire de la chaire de neurologie à l'université de l’Arizona, a annoncé les résultats de l'étude FORTITUDE-ALS (résultats fonctionnels d'un essai randomisé de traitement d'investigation avec CK-2127107)
FORTITUDE-ALS n’a pas atteint la signification statistique pour une relation dose-réponse pré-spécifiée dans son critère de jugement principal du changement de la capacité vitale lente (VCS) après 12 semaines d’administration (p = 0,11). Des analyses similaires de ALSFRS-R et de la pente du Mega-Score de force musculaire ont donné respectivement des valeurs de p de 0,09 et 0,31. Cependant, les patients dans les groupes de traitement par Reldesemtiv ont moins régressé que les patients sous placebo pour ce qui est de la CVS et de l'ALSFRS-R, des différences plus importantes et cliniquement significatives apparaissant avec le temps.
Bien que les analyses dose-réponse pour les critères d'évaluation principaux et secondaires n'atteignent pas une signification statistique de 0,05, dans une analyse post-hoc regroupant les doses, les patients qui ont reçu Reldesemtiv dans FORTITUDE-ALS ont moins régressé que les patients qui ont reçu un placebo. L'essai a montré des effets favorisant les réactions reliant les doses et les moments, avec des amplitudes cliniquement significatives observées à 12 semaines pour les critères d'évaluation principaux et secondaires. Les différences entre le score Reldesemtiv et le placebo entre la CVS et le score total ALSFRS-R observées après 12 semaines de traitement étaient toujours évidentes au suivi, quatre semaines après la dernière dose du médicament à l'étude.
L'incidence des abandons précoces du traitement, des effets indésirables graves et des effets indésirables cliniques observés dans FORTITUDE-ALS était similaire entre le groupe placebo et le groupe de traitement actif. La fatigue, les nausées et les maux de tête ont été les effets indésirables les plus fréquents au cours de l’essai. La principale cause de terminaison précoce de FORTITUDE-ALS chez les patients recevant un placebo était une maladie évolutive; la principale cause d'arrêt précoce chez les patients traités par Reldesemtiv était une diminution du débit de filtration glomérulaire estimé (C-GF) basé sur la cystatine C, une mesure de la fonction rénale. Les élévations des transaminases et les baisses du DFGP de la cystatine C étaient liées à la dose.
“Les résultats de FORTITUDE-ALS sont parmi les plus impressionnants que nous ayons vus au cours d’un essai clinique de phase 2 sur la SLA," a déclaré le Dr Shefner. "La cohérence et la durabilité des effets observés dans tous les données de traitement sur des paramètres significatifs sur le plan clinique sont particulièrement remarquables."
En collaboration avec Astellas, Cytokinetics développe actuellement Reldesemtiv, un activateur rapide de la troponine du muscle squelettique (FSTA) de nouvelle génération, comme traitement potentiel pour les personnes atteintes de maladies débilitantes et de conditions associées à une faiblesse et / ou une fatigue du muscle squelettique.
Point de terminaison d'efficacité principal et analyses supplémentaires
Dans FORTITUDE-ALS, l’analyse principale de la variation de la CVS prévue en pourcentage entre le début de la semaine et la semaine 12 a été analysée à l’aide d’un modèle mixte pour mesures répétées (MMRM) avec le contraste (-5, -1, 3, 3) afin de refléter la pondération supposée. relation dose-réponse pour les groupes recevant respectivement 150 mg BID, 300 mg BID et 450 mg BID du placebo, respectivement. Alors que toutes les doses de Reldemtiv ont démontré des réductions numériques de la CVS par rapport au placebo, l'analyse du modèle mixte n'était pas statistiquement significative (p = 0,11) (Figure 1). Dans une analyse post-hoc, lorsque tous les groupes de traitement actifs ont été combinés et comparés au placebo, l’essai a montré une réduction de 27% du déclin de la CVS (p = 0,10) (Figure 2).
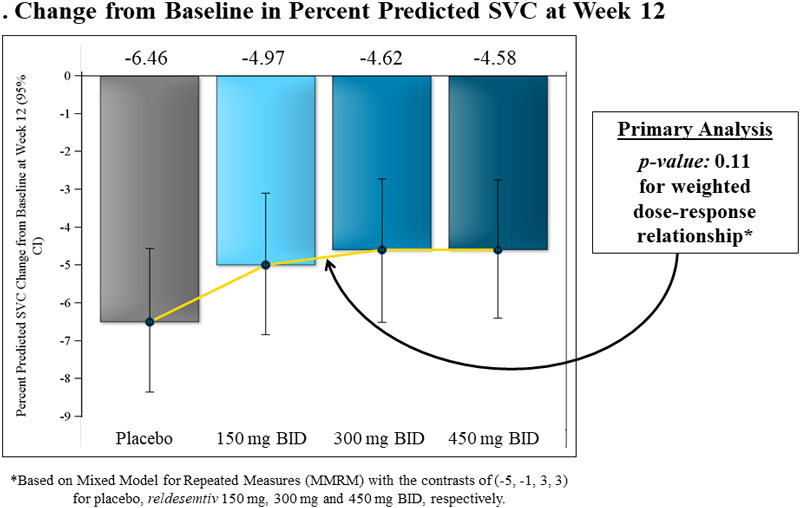
Variation par rapport au niveau de référence du pourcentage de CVS prédit à la semaine 12

Changement de SVC à partir de la ligne de base (All Active vs Placebo)
Dans FORTITUDE-ALS, le taux de diminution de la CVS dans le groupe placebo a été plus lent que celui observé dans les essais précédents. FORTITUDE-ALS était sous tension, les patients sous placebo risquant alors de perdre environ 8,0 points de pourcentage au cours des 12 semaines d’essai. Dans FORTITUDE-ALS, le nombre de patients sous placebo a diminué de 6,5 points de pourcentage sur 12 semaines.
Critères d'évaluation secondaires de l'efficacité: analyses supplémentaires
Dans une analyse post-hoc, FORTITUDE-ALS a démontré une diminution du déclin de l'ALSFRS-R par rapport aux valeurs initiales à 12 semaines à 25% (p = 0,01) lorsque tous les groupes de traitement actifs ont été comparés au placebo (Figure 3). Le système ALSFRS-R mesure les activités de la vie quotidienne et a été jugé acceptable par les autorités de régulation pour approbation et autorisation de mise sur le marché. Selon un sondage mené en 2010 par le Northeast ALS clinicians (ALS) auprès de cliniciens SLA, les personnes interrogées ont estimé qu'un traitement ayant entraîné une modification d'au moins 20% à 25% de la pente de déclin de ALSFRS-R était un effet cliniquement significatif.
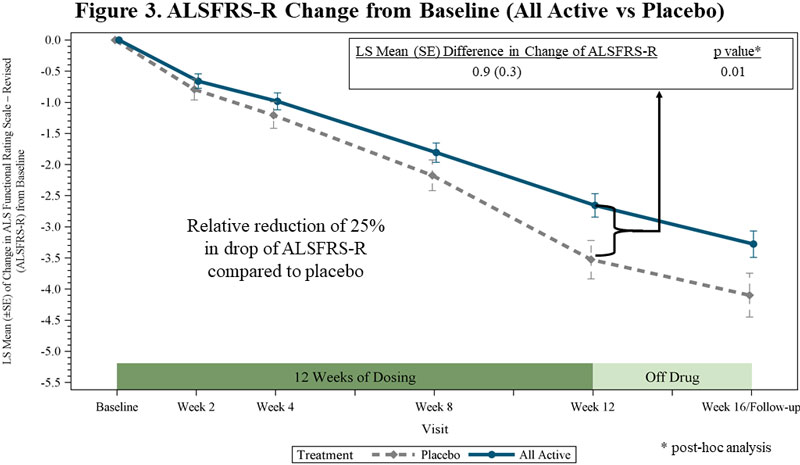
Variation ALSFRS-R par rapport à la valeur de base (tous les actifs par rapport au placebo)
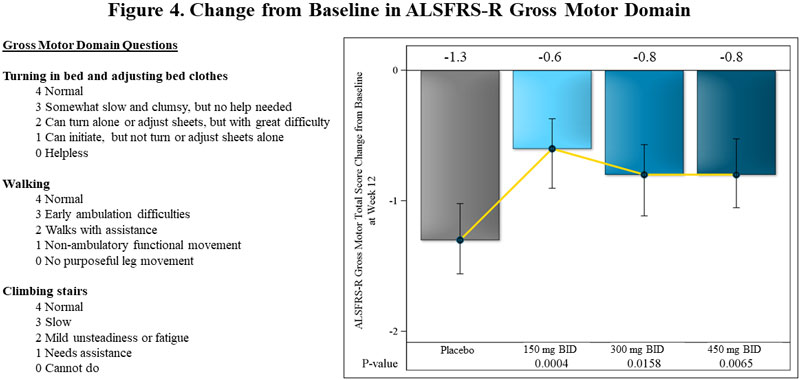
Changement du niveau de référence dans le domaine moteur global ALSFRS-R
Dans les domaines ALSFRS-R, les effets les plus importants observés à 12 semaines dans FORTITUDE-ALS ont été observés dans le domaine de la motricité globale de l'ALSFRS-R, qui mesure la capacité des patients atteints de SLA à se retourner au lit, à marcher et à monter les escaliers. L'effet de Reldesemtiv sur le score de motricité globale était statistiquement significatif pour chaque dose versus placebo (p = 0,0004 pour 150 mg BID, p = 0,0158 pour 300 mg BID, p = 0,0065 pour 450 mg BID) (Figure 4).
“Bien que FORTITUDE-ALS n’ait pas atteint le critère principal, nous sommes encouragés par les résultats de l’essai, car ils confirment le potentiel d’activation des muscles squelettiques dans le traitement des patients SLA," a déclaré Fady I. Malik, MD, Ph.D., Vice-président exécutif de la Recherche et développement de Cytokinetics. "Cet essai de phase 2 de Reldesemtiv a démontré la cohérence de l'effet pour les doses, les paramètres d'effet et les points de temps, et nous pensons que les résultats corroborent l'évolution de Reldesemtiv au cours d'essais cliniques ultérieurs conduisant à un enregistrement potentiel."
Traduction : Christina Lambrecht
Source : Cytokinetics, Incorporated


