Le troisième médicament antisense innovateur d'Ionis pour la SLA, le premier conçu pour traiter une large population de patients SLA, commence un essai clinique
26-10-2020
- L'essai évaluera ION541 (BIIB105) pour le traitement de la plupart des formes de SLA indépendamment des antécédents familiaux
- Tofersen et IONIS-C9Rx sont actuellement également en essais cliniques ciblant les formes génétiques de la maladie
CARLSBAD, Californie, USA - Ionis Pharmaceuticals, le leader de la thérapie antisense, a annoncé aujourd'hui que les premiers patients ont reçu le ION541 (également connu sous le nom de BIIB105), un médicament antisense expérimental en cours de développement comme thérapie potentielle pour traiter la plupart des formes de la sclérose latérale amyotrophique (SLA) indépendamment des antécédents familiaux. Il s'agit d'une autre étape importante du progrès continu du programme ambitieux d'Ionis visant à développer de nouveaux traitements contre la SLA. Presque tous les cas de SLA partagent la caractéristique pathologique de l'agrégation des protéines TDP-43 dans les motoneurones. ION541 cible l'ARN de l'ataxine-2 (ATXN2), dont il a été démontré qu'il prévient ou inverse la toxicité du TDP-43 dans les modèles précliniques de la SLA.
Traduction : Ligue SLA : Anne
Source : PR Newswire
De la molécule à l’humain : la découverte de gènes mène à une thérapie expérimentale de nouvelle génération pour la SLA
28-10-2020
Auteur : Julie Kiefer
Après plus de 25 ans dans la fabrication, les découvertes scientifiques faites par Stefan Pulst, MD, Dr Med et son équipe de recherche ont franchi le cap des essais cliniques humains avec un traitement unique pour le syndrome latéral amyotrophique (SLA). Le médicament expérimental fait partie d’une nouvelle classe de thérapies de nouvelle génération qui s’attaquent à la cause fondamentale de la maladie – le code génétique – et se révèlent prometteuses pour soulager des conditions auparavant incurables.

Des découvertes du laboratoire de Stefan Pulst, Dr Med, sur une maladie rare, l’ataxie, ont mené à un médicament potentiel pour une autre condition neurologique dévastatrice, la SLA. Crédit photo : Charlie Ehlert.
C’est un pas en avant encourageant pour la SLA une perte rapide et progressive de la fonction des cellules du système nerveux. Aujourd’hui, les patients ont une espérance de vie moyenne de seulement deux à cinq ans après le diagnostic, et aucun médicament ne peut ralentir ou arrêter la maladie.
‘’C’est un changement radical’’, dit Pulst. ‘’C’est le premier composé du genre pour tous les types de SLA, génétiques et sporadiques. Nous espérons que dans 10 ans, nous en parlerons comme nous faisons aujourd’hui des thérapies ciblées contre le cancer.’’
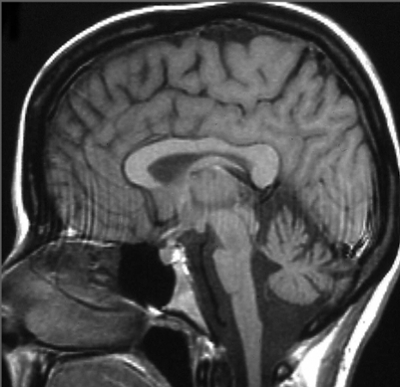
Image IMR montrant atrophie du cervelet et du tronc cérébral chez un patient avec ataxie spinocérébelleuse type 2.
Dans les années 1990, Pulst ne pouvait pas savoir que rencontrer une famille avec un trouble du système nerveux différent – l’ataxie – ouvrirait la voie à la nouvelle thérapie d’essai pour la SLA. Après avoir appris l’existence de la famille d’un collègue médical, Pulst a traversé le pays du Cedars-Sinai Medical Center à Los Angeles, où il était président de la neurologie, à l’état de New York pour examiner les membres de la famille et recueillir des échantillons pour analyse. La rencontre a lancé une enquête de cinq ans qui a abouti à la découverte de changements dans un gène, l’ataxine-2, qui a provoqué leur ‘malédiction familiale’, maintenant appelée ataxie spinocérébelleuse de type 2. La même condition génétique a également été trouvée dans des familles non-apparentées autour du monde.
Une décennie plus tard, Pulst a déménagé à l’U of U Health en tant que président du département de neurologie, où il a poursuivi des recherches pour acquérir une compréhension approfondie de ce qui ne va pas dans le corps au cours de l’évolution de la maladie. Avec son proche collaborateur, Daniel Scoles, PhD, professeur agrégé de neurologie, il a développé des souris atteintes d’une maladie de type ataxie, fournissant un moyen de découvrir des gènes et des voies biochimiques qui deviennent perturbés avec le temps. Le modèle de la maladie a également joué un deuxième rôle critique, parce qu’il exprimait le gène mutant de l’ataxine-2 humaine, il est devenu un outil pour tester des thérapies ciblées sur le gène.

Recherche par Stefan Pulst, Dr Med, et Daniel Scoles, PhD, a démontré qu’une thérapie avancée inverse un trouble semblable à la SLA dans les animaux. Crédit photo : Charlie Ehlert.
Pulst et Scoles ont collaboré avec Ionis Pharmaceuticals pour poursuivre une nouvelle approche de traitement qui a commencé à se montrer prometteuse pour d’autres affections neurodégénératives. Ils ont démontré qu’un type de médicament, connu sous le nom d’antisens, réduisait l’expression du gène de l’ataxine-2 et ralentissait la progression de l’état de type ataxie des animaux. Les souris ont obtenu de meilleurs résultats d’équilibre et de coordination et ont montré des signes de récupération au niveau cellulaire. Le médicament antisens est une molécule de type ADN synthétisée chimiquement qui cible l’ARNm de l’ataxine-2, entraînant sa destruction.
Dans une découverte surprise, une deuxième étude a montré qu’un médicament antisens similaire contre l’ataxine-2 améliorait également la santé des souris atteintes d’une maladie de type SLA. Dans ce cas, l’effet était indirect, réduisant l’agglutination toxique d’une autre protéine connue pour être impliquée dans la SLA. Le traitement a considérablement prolongé la vie des souris SLA.

Les essais cliniques sont un jalon fondé sur des décennies de recherche. Ici photo de membres du laboratoire de Pulst, Sharan Paul, PhD, et Warunsee Dansithong, PhD. Crédit photo : Charlie Ehlert.
C’était une preuve de concept que ces composés pourraient devenir la base de nouvelles thérapies pour les maladies neurodégénératives, qui jusqu’à présent ont été largement impénétrables’’, explique Pulst. Avec le soutien des National Institutes of Health, Pulst, Scoles et Ionis Pharmaceuticals ont encore affiné le traitement, trouvant un médicament antisens qui a bien fonctionné dans les études animales avec une sécurité et une efficacité inégalées. Sur la base de ces résultats, la FDA américaine a autorisé les essais sur l’homme. Les essais de sécurité clinique de phase 1 du médicament, appelés BIIB105, sont parrainés par Biogen et commencent à recruter des patients le 2 septembre.
‘’Un de mes professeurs m’a dit qu’il était rare que quelqu’un fasse une différence significative dans le domaine de la science’’, dit Scoles. ‘’Mais, nous n’avons jamais cessé d’essayer. Espérons que ce médicament fasse une différence significative.’’
Traduction : Gerda Eynatten-Bové
Source : University of Utah Health


