Een genmutatie die ALS vertraagt of versnelt
10-04-2020
Wetenschappers hebben ons nieuwe inzichten geboden in de manier waarop mutaties in het gen TBK1 aan de basis liggen van amyotrofische laterale sclerose (ALS), een progressieve neurodegeneratieve ziekte die patiënten belemmert in hun bewegingen en spraak en uiteindelijk tot de dood leidt. De onderzoekers kwamen tot de vaststelling dat met ALS geassocieerde mutaties in TBK1 zowel positieve als negatieve effecten kunnen hebben op het verloop van de ziekte bij muizen die dusdanig genetisch werden bewerkt dat ze op ALS gelijkende symptomen vertonen.
Deze bevindingen werden gerapporteerd in Neuron en bieden zowel genetische als mechanistische inzichten die zouden kunnen leiden tot nieuwe strategieën voor de ontwikkeling van behandelingen voor ALS.
"Een van de grootste uitdagingen bij het vinden van een genezing voor ALS is gebruik te maken van genetische gegevens om de onderliggende mechanismen van de ziekte te doorgronden”, zegt de hoofdauteur van de studie. "Bij neurodegeneratieve ziektes als ALS zijn bijvoorbeeld meerdere celtypes betrokken die voortdurend veranderen naarmate de ziekte voortschrijdt, zodat een geneesmiddel dat werkt in de vroege ziektestadia later schadelijk zou kunnen blijken te zijn. Onze studie licht een tipje van de sluier op die de complexe verhouding verhult tussen de genetica van ALS en de mechanismen ervan. Ze zet ook de uitdaging in de verf van de ontwikkeling van veilige en effectieve geneesmiddelen om de ziekte te behandelen", aldus de auteur.
ALS is een ziekte van het ruggenmerg, die op gang kan worden gebracht door de accumulatie van misgevouwen eiwitten in motorneuronen, de zenuwcellen in het ruggenmerg die de bewegingen sturen.
Het menselijke TBK1-gen is één van meer dan 25 genen waarvan we weten dat ze verband houden met of de oorzaak zijn van ALS wanneer ze drager zijn van een mutatie. TBK1 is een centrale speler bij meerdere celfuncties, waaronder autofagie, een proces dat misgevouwen eiwitten, beschadigde stukjes cel en bacteriële pathogenen verwijdert. TBK1 is ook vereist voor de antimicrobiale interferonrespons, die cellen beschermt tegen bacteriële en virale infecties.
"TBK1 helpt cellen bij het verwijderen van klonters misgevouwen eiwitten en beschermt het lichaam tegen invasieve virussen en bacteriën", zegt de hoofdauteur van de studie. "En aangezien individuen met bepaalde mutaties in TBK1 ALS blijken te hebben, wilden we tot een diep, mechanistisch begrip komen van de manier waarop deze mutaties in de loop van de ziekte de celfuncties in het ruggenmerg aantasten."
De auteurs brachten ALS-veroorzakende TBK1-mutaties in bij muizen. Deze muizen vertoonden geen tekenen van ALS.
"Dat was geen verrassing, aangezien slechts enkele van de vele ALS-mutaties die tot dusver door andere ALS-onderzoekers werden getest bij muizen resulteerden in ALS", zegt de hoofdauteur.
Om dit probleem te omzeilen, brachten de onderzoekers TBK1-mutaties in bij een muizenmodel waarvan vastligt dat het ALS heeft, de SOD1-muis. Daarna controleerden ze het ziekteverloop bij deze muizen.
Deze nieuwe muizen vertoonden opvallende verschillen op het gebied van het ziekteverloop vergeleken met muizen die alleen drager zijn van de SOD1-mutaties. Meer specifiek ving de ziekte eerder aan.
"We stelden vast dat muizen die drager waren van zowel de SOD1- als de TBK1-mutaties eerder last kregen van abnormale bewegingen dan muizen die alleen drager waren van de SOD1-mutaties", aldus de hoofdauteur. "Nader onderzoek van de muizen bracht ook eerder dan verwacht schade aan motorneuronen en het verlies van spierconnecties aan het licht."
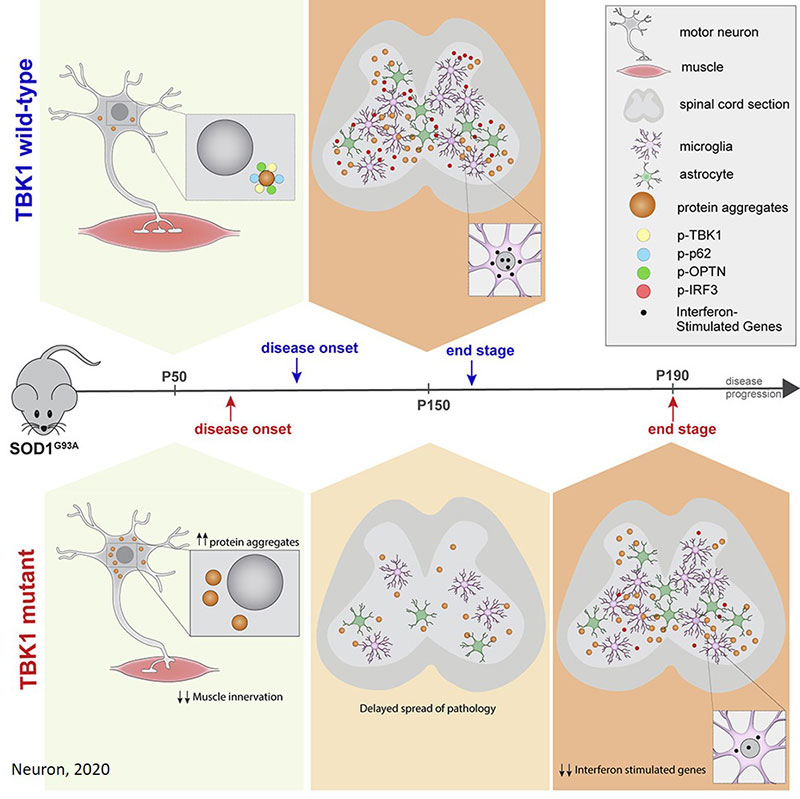
Om dit fenomeen verder te bestuderen, onderzochten de wetenschappers een andere groep van SOD1-ALS-muizen, waarbij het TBK1-gen was uitgeschakeld in motorneuronen, maar niet in andere cellen van het ruggenmerg. Het team stelde vast dat de afwezigheid van TBK1-activiteit in motorneuronen als dusdanig leidde tot het wegvallen van autofagie in deze cellen. Dit leidde dan weer tot een toename van de accumulatie van schadelijke eiwitten, een vroegere motorneuronendood, en een verlies van neuron-spierconnecties. Deze vaststellingen toonden aan dat een vroegere ziekteaanvang een gevolg was van het ontbreken van TBK1 in motorneuronen.
Paradoxaal genoeg echter vertraagde het ziekteverloop in een later stadium van de ziekte en leefden muizen met een TBK1-functieverlies in alle cellen 25 percent langer dan zowel de muizen die alleen drager waren van SOD1, als de muizen waarbij het TBK1-gen alleen was uitgeschakeld in motorneuronen.
Daarop onderzocht het team de precieze manier waarop TBK1-mutaties invloed uitoefenen op andere cellen in het ruggenmerg. De onderzoekers ontdekten dat de interferonrespons werd onderdrukt in gliale cellen, meer bepaald astrocyten en microglia. Hoewel de interferonrespons cruciaal is voor de afweer tegen infecties bij gezonde mensen, kan hij bij overproductie (wat het geval is bij ALS-muizen) toxisch zijn en een stortvloed van celprocessen op gang brengen die toxisch zijn voor motorneuronen.
"Het wegvallen van TBK1 in microglia en astrocytes vermindert duidelijk de interferonrespons in het ruggenmerg van ALS-muizen", zegt de hoofdauteur. "Dit correleert met een significante verlenging van hun leven."
"Onze studie biedt een voorbeeld van de manier waarop meerdere trajecten in en tussen cellen als doelwit kunnen worden gekozen via de manipulatie van één enkel gen en van de manier waarop een wijziging van deze trajecten bij ALS weldadig – of schadelijk – kan uitpakken in verschillende stadia van het ziekteverloop", voegt de auteur eraan toe.
De hoofdauteur stelt dat dit type van fundamenteel, door ontdekkingen gedreven onderzoek zal leiden tot behandelingen die zich toespitsen op de onderliggende mechanismen van ALS en de slopende symptomen ervan.
"Uiteindelijk liggen genen aan de basis van alle neurodegeneratieve ziektes", besluit de hoofdauteur. "Naarmate we meer cruciale genetische informatie verzamelen, kunnen we mutaties identificeren – zoals die in TBK1 – die bijkomende mechanistische inzichten zullen opleveren. Deze genen en de trajecten die ze controleren zullen cruciaal zijn voor de ontwikkeling van geneesmiddelen die een verschil zullen maken in het leven van ALS-patiënten."
Vertaling: Bart De Becker
Bron: Science Mission


