Is er een genetische schakelaar die ALS veroorzaakt?
23-10-2015
Ben Locwin
In de zomer van 2014 ging de Ice Bucket Challenge van start om Amyotrofische Laterale Sclerose (ALS) onder de aandacht te brengen. Het werd een populair fenomeen op sociale media. 440 miljoen mensen bekeken in totaal 10 miljard keer de video’s van deelnemers aan de Ice Bucket Challenge. Het resultaat: de ziekte werd bekender bij het publiek, de ALS Association kon haar uitgaven voor onderzoek verdrievoudigen en het aantal donaties ging de hoogte in. Het fenomeen wordt ieder jaar in augustus herhaald (#ALSIceBucketChallenge).
ALS is een neurologische aandoening die de zenuwcellen aantast die willekeurige spieren in het lichaam controleren. Meestal vordert de ziekte snel. Volgens de ALS Association overlijdt de patiënt binnen de 2 tot 5 jaar. In ongeveer 90 procent van de gevallen kunnen onderzoekers nog steeds geen oorzaken van de aandoening vinden, maar bij 10 procent van de patiënten zou ALS erfelijk bepaald zijn.
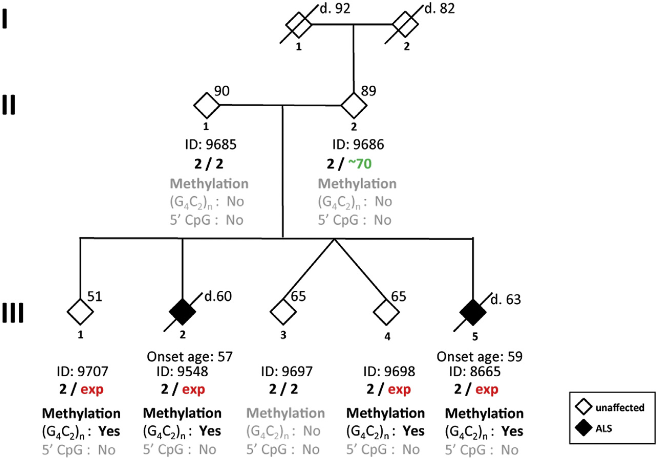
Een nieuwe onderzoekslijn, gepubliceerd in American Journal of Human Genetics, heeft het voornamelijk over het gen C9orf72. Mutaties in dit gen kunnen namelijk in verband gebracht worden met een instabiele DNA-sequentie die, met genoeg herhalingen, geassocieerd kan worden met het ontstaan van ALS. Het recent gepubliceerde onderzoek focust op drie generaties van een familie en richt zich op het gen C9orf72 en de herhalingen. Interessant genoeg kregen noch de grootouders noch de ouders van de derde generatie in het onderzoek te maken met ALS, maar bij 4 van de 5 nakomelingen in de derde generatie werd de ziekte vastgesteld.
In de studie had de vader 70 niet-gemethyleerde herhalingen en bij de kinderen met ALS werd een mutatie vastgesteld die tot meer dan 1.000 gemethyleerde herhalingen had. Volgens de onderzoekers kon er dus worden vastgesteld dat ergens tussen de onder- en overexpressie van het gen C9orf72 en de 70 tot 1.000 herhalingen, er bij de vader geen ALS ontstond en bij de volwassen kinderen wel. Er wordt zo gesuggereerd dat er ergens een drempel is die een genetische schakelaar activeert, waardoor de ziekte tot uiting komt.
Een andere factor is dat C9orf72 wordt gevonden in het kernmembraan in normale gezonde neuronen, maar niet in zieke neuronen — daar worden ze door translocatie teruggevonden in het plasmamembraan van de neuronale cel. Dit is een belangrijk gegeven, vermits het eiwitverkeer in het kernmembraan van de cel (de celkern is omgeven door dit membraan) wordt afgeremd als C9orf72 is verplaatst.
Het transport van het eiwit TDP-43 verloopt niet correct bij ALS-patiënten en de accumulatie van TDP-43 in de intercellulaire vloeistof is, naast andere veranderingen in de eiwitten, een kenmerk bij ALS. Het was al een tijd geweten dat TDP-43 (TAR DNA-bindend eiwit, 43 kilodalton — om de omvang uit te drukken) in verband wordt gebracht met wijzigingen in de eiwitten die met ALS en fronto-temporale dementie worden geassocieerd, maar de vermoedelijke oorzakelijke factor van het gen C9orf72 en de besproken herhalingen zijn belangrijke nieuwe factoren in het onderzoek naar ALS. De onderzoekers stelden het volgende vast:
“De ziektemechanismen die gerelateerd zouden zijn aan C9orf72 zijn complex... bij personen met uitbreidingen zijn ~50% minder transcripties van C9orf72 gevonden, mogelijk als gevolg van epigenetische alteraties... Bovendien werd een hogere mate van methylatie in verband gebracht met familiale ALS en een kortere ziekteduur.”
Bron: University of Toronto
Interessant genoeg hebben onderzoekers gesuggereerd dat de epigenetische methylatieveranderingen van de herhalingsuitbreiding “een beschermingsmechanisme is om de productie van toxisch RNA en toxische dipeptiden, die tot bijkomende schade kunnen leiden, te beperken”. Evenzo werden methylaties in verband gebracht met een afgenomen expressie van het gen C9orf72.
ALS wordt doorgaans niet in verband gebracht met cognitieve achteruitgang. Als bekend voorbeeld wordt ALS-patiënt Stephen Hawking vaak aangehaald om aan te tonen dat zijn hersenen, ondanks zijn fysieke achteruitgang, nog steeds op een uitermate hoog niveau blijven functioneren. Er zijn echter ook gevallen bekend van geheugenverlies en depressie bij ALS-patiënten.
Het moeilijke bij het bepalen van de oorzaken van depressies en geheugenproblemen is het feit dat aanzienlijke fysieke en psychologische stress (die kan gepaard gaan bij het ontstaan van ALS) zowel depressies en geheugenverlies in de hand kunnen werken. Of er zou zelfs sprake kunnen zijn van een keten van oorzaak en gevolg, waarbij de stress van de ziekte leidt tot depressie, wat op zich een bekende voorloper is van (of vaak samengaat met) geheugenproblemen. Of omgekeerd, wanneer de ziekte de cognitieve vaardigheden van de patiënt aantast door stress en angst waardoor de ziekte en het geheugenverlies leidt tot depressie.
De volgende onderzoekslijn voor dit onderzoek zou er dan in bestaan om de verkregen resultaten te bekrachtigen, door verschillende generaties van bijkomende families te analyseren en te kijken in welke mate de bevindingen kloppen. Op die manier zullen onderzoekers ook meer gegevens kunnen verzamelen over het aantal DNA-herhalingen die wel of niet in verband gebracht worden met het al dan niet ontstaan van ALS. Zo zullen we het aantal herhalingen in kaart kunnen brengen dat waarschijnlijk in verband wordt gebracht met het ontstaan van ALS – tenminste in een aantal gevallen.
Het probleem is nog niet van de baan, maar het begrijpen van de onderliggende genetische en biologische mechanismen die een rol spelen, maakt het mogelijk om de ziekte beter te voorkomen of te genezen en om de diagnostiek te verbeteren, zodat mensen betere mogelijkheden hebben om te weten hoe ze met de ziekte kunnen omgaan.
Vertaling: Barbara Bastiaansen
Bron: Genetic Literacy Project


