Utilisation de L'imagerie Multimodale et des Biomarqueurs Cliniques dans les Porteurs Présymptomatiques de l'Expansion Répétée de C9orf72
20-05-2020
Joke De Vocht, Jeroen Blommaert, Martijn Devrome, Ahmed Radwan, Donatienne Van Weehaeghe, Maxim De Schaepdryver, Jenny Ceccarini, Ahmadreza Rezaei, Georg Schramm, June van Aalst, Adriano Chiò, Marco Pagani, Daphne Stam, Hilde Van Esch, Nikita Lamaire, Marianne Verhaegen, Nathalie Mertens, Koen Poesen, Leonard H. van den Berg, Michael A. van Es, Rik Vandenberghe, Mathieu Vandenbulcke, Jan Van den Stock, Michel Koole, Patrick Dupont, Koen Van Laere, Philip Van Damme
Points clés
Question
Des changements métaboliques cérébraux peuvent-ils être détectés chez des individus pré-symptomatiques porteurs d'une expansion répétée de l'hexanucléotide dans le gène C9orf72 (preSxC9) en utilisant une imagerie tomographique et une imagerie par résonance magnétique et une imagerie par résonance magnétique, du fluorodeoxyglucose marqué au fluor en temps 18 et quelle est l'association entre la mutation et les biomarqueurs cliniques et fluides de la sclérose latérale amyotrophique et de la démence frontotemporale?
Résultats
Dans une étude cas-témoins incluant 17 participants préSxC9 et 25 témoins sains, l'imagerie tomographique par émission de positons au fluorodeoxyglucose marqué au fluor 18 a noté des grappes importantes d'hypométabolisme relatif dans les régions frontotemporales, les cortex insulaires, les noyaux gris centraux et les thalami chez les participants préSxC9. L'utilisation de cette stratégie a permis de détecter des changements au niveau individuel.
Signification
Les changements métaboliques du glucose semblent se produire au début de la séquence d'événements conduisant à une sclérose latérale amyotrophique manifeste et à une démence frontotemporale. L'imagerie tomographique par émission de positons au fluorodésoxyglucose marquée au fluor 18 peut fournir un biomarqueur sensible d'une phase présymptomatique de la maladie.
Abstrait
Importance
À une époque où il existe un potentiel pour de nouvelles stratégies de traitement, la détection précoce des manifestations de la maladie au niveau individuel chez les porteurs présymptomatiques d'une expansion répétée hexanucléotidique du gène C9orf72 (preSxC9) devient de plus en plus pertinente.
Objectifs
Évaluer les changements dans le métabolisme du glucose avant l'apparition des symptômes de la sclérose latérale amyotrophique ou de la démence frontotemporale dans la préSxC9 en utilisant simultanément du fluorodésoxyglucose marqué au fluor 18 ([18F] FDG, émission tomographique (PET) et imagerie par résonance magnétique, ainsi que l'association de la mutation avec la clinique et biomarqueurs fluides.
Conception, cadre et participants
Une étude prospective cas-témoins a recruté 46 participants de 30 novembre 2015 au 11 décembre 2018. L'étude a été menée au centre de référence neuromusculaire des Hôpitaux Universitaires de Louvain, Louvain, Belgique.
Principaux résultats et mesures
Les données de neuroimagerie ont été normalisées spatialement et analysées au niveau du voxel à un seuil de hauteur de P <0,001, au seuil corrigé des erreurs au niveau de la famille de P <0,05 et la signification statistique a été fixée à P <0,05 pour l'analyse du niveau de volume d'intérêt, en utilisant la correction de Benjamini-Hochberg pour une correction multiple. Les cartes de score W ont été calculées en utilisant les individus servant de témoins comme référence pour quantifier le degré d'anomalie de la TEP [18F] FDG. Le seuil d'anomalie sur les cartes de score W a été désigné comme un score W absolu supérieur ou égal à 1,96. Les niveaux et les performances des neurofilaments aux examens cognitifs et neurologiques ont été déterminés. Tous les tests d'hypothèse étaient unilatéraux.
Résultats
Sur les 42 participants inclus, 17 étaient porteurs de la mutation preSxC9 (12 femmes [71%]; âge moyen [ET], 51 [9] ans) et 25 témoins sains (12 femmes [48%]; moyenne [ET] âge, 47 [10] ans). Comparativement aux participants témoins, des grappes importantes d'hypométabolisme relatif ont été trouvées dans les régions frontotemporales, les noyaux gris centraux et les thalami des participants préSxC9 et un hypermétabolisme relatif dans la région péri-rolandique, le gyrus frontal supérieur et le cortex précuneus. Les cartes de fréquence des scores W ont révélé une réduction du métabolisme du glucose avec des maxima locaux dans les cortex insulaires, le cortex operculaire central et les thalami chez jusqu'à 82% des participants préSxC9 et une augmentation du métabolisme du glucose dans le gyrus précentral et le cortex précuneus dans jusqu'à 71% des participants préSxC9. D'autres résultats dans le groupe preSxC9 étaient une atteinte des motoneurones supérieurs chez 10 participants (59%), des anomalies cognitives chez 5 participants (29%) et des niveaux élevés de neurofilaments chez 3 des 16 personnes (19%) ayant subi une ponction lombaire.
Conclusions et pertinence
Les résultats suggèrent que la TEP [18F] FDG peut identifier les changements métaboliques du glucose dans preSxC9 à un niveau individuel, précédant des niveaux de neurofilament significativement élevés et l'apparition de symptômes.
Traduction : Christina Lambrecht
Source : JAMA Neurology
![]()
Use of Multimodal Imaging and Clinical Biomarkers - JAMA Neurology
Chercheurs de Leuven (Louvain) réussissent dans la détection précoce de la SLA et de la démence frontotemporale
 Leuven - Avec un PET-scan spécifique, des chercheurs liés à la VIB-KU Leuven et UZ Leuven ont réussi à détecter, chez des personnes avec des mutations au gène C9orf72, des changements cérébraux avant même d’être malades. Selon le neurologue Philip Van Damme, ceci est une percée importante, qui peut aider à déterminer quand il est le plus opportun de commencer avec des traitements préventifs.
Leuven - Avec un PET-scan spécifique, des chercheurs liés à la VIB-KU Leuven et UZ Leuven ont réussi à détecter, chez des personnes avec des mutations au gène C9orf72, des changements cérébraux avant même d’être malades. Selon le neurologue Philip Van Damme, ceci est une percée importante, qui peut aider à déterminer quand il est le plus opportun de commencer avec des traitements préventifs.
Des mutations au gène C9orf72 sont la cause la plus courante de démence frontotemporale héréditaire (DFT) et de la maladie musculaire SLA.
DFT est, après la maladie de Alzheimer, la forme la plus courante de démence à un jeune âge. La plupart des patients SLA meurent endéans les deux à cinq ans après les premiers symptômes.
Que cette mutation de gène conduit à ces deux maladies différentes fait supposer, selon Van Damme, que plusieurs facteurs peuvent influencer le processus de la maladie en sens positif ou négatif. ‘’ Ces facteurs pourraient être des cibles thérapeutiques intéressantes’’, selon le neurologue.
Joke De Vocht du Labo de Van Damme a étudié, chez les porteurs de la mutation du gène nommé, à l’aide d’une imagerie avancée (imagerie avancée time-of-flight 18F FDG-PET MR), la phase pré-symptomatique et a réussi à identifier, sur le niveau individuel, des changements même avant que les premiers signes de la maladie ne surgissent.
Se référant aux nouvelles stratégies de traitement qui sont en développement pour ralentir la maladie, ou même la prévenir, cette percée est, selon Van Damme, très importante. ‘’Ceci peut aider à déterminer quand il est le plus opportun d’intervenir avec des traitements préventifs’’, dixit le neurologue.
Traduction : Gerda Eynatten-Bové
Source : MediQuality
Le scan TEP montre des signes précoces de changements du métabolisme du glucose chez les porteurs asymptomatiques de mutation pour la SLA et la démence frontotemporale
16-07-2020
Article en bref
Les examens TEP de porteurs asymptomatiques de l'hexanucléotide répètent l'expansion dans le gène du cadre de lecture ouvert 72 du chromosome 9 - impliqué à la fois dans la sclérose latérale amyotrophique et la démence frontotemporale - ont montré des changements dans le métabolisme du glucose. Les résultats suggèrent que ces altérations métaboliques du glucose pourraient potentiellement présager des signes précoces des deux maladies.
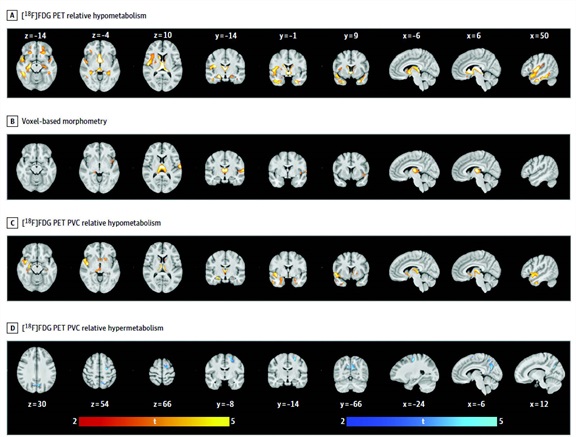
Des changements dans le métabolisme du glucose ont été détectés dans les balayages TEP de porteurs asymptomatiques d'une expansion répétée hexanucléotidique du gène du cadre de lecture ouvert 72 (C9ORF72) du chromosome 9, par rapport à des témoins sains, selon un rapport publié dans le numéro en ligne du 18 mai de JAMA Neurology.
Les personnes présentant des expansions répétées du gène peuvent finalement développer une démence frontotemporale (FTD), une sclérose latérale amyotrophique (SLA), ou les deux. Les raisons pour lesquelles certaines personnes développent l'une de ces maladies, ou les deux, ne sont pas claires.
Pour la présente étude, l'équipe de recherche a testé des porteurs asymptomatiques de l'expansion répétée (issus de familles ayant des mutations connues) avec un certain nombre de biomarqueurs - scintigraphies cérébrales, examens cliniques et neurologiques, examens neuropsychologiques et niveaux de neurofilaments dans le liquide céphalorachidien (LCR) - rechercher les changements qui pourraient aider à comprendre ce qui se passe au cours des étapes précédant l'apparition des symptômes.
"Cette étude montre qu'il peut y avoir une longue fenêtre d'opportunité à des fins de diagnostic et pour les traitements précoces, lorsqu'ils deviennent disponibles", a déclaré Philip Van Damme, MD, PhD, auteur principal de l'étude, et doctorante Joke De Vocht, MSc, tous deux aux hôpitaux universitaires de Louvain en Belgique.
"L'étude de la séquence des événements qui se produisent avant le début de la maladie clinique sera de la plus haute importance pour mieux comprendre les stades prodromiques de la maladie et prédire les présentations de la maladie clinique", a-t-il ajouté.
Ces mutations C9ORF72, identifiées pour la première fois en 2011 par deux équipes indépendantes de scientifiques de la Mayo Clinic et du National Institute on Aging, représentent environ 34% des cas de SLA familiale, près de 6% des cas de SLA sporadiques, un quart des FTD familiaux. et 5% des cas de FTD sporadiques.
Méthodes d'étude, résultats
Le Dr Van Damme a commencé à étudier les familles avec des mutations C9ORF72 il y a une dizaine d'années. Pour l'étude actuelle, entre 2015 et 2018, lui et ses collègues ont sélectionné 42 participants pour l'étude; 17 portaient l'expansion répétée du gène C9ORF72 et ont été comparés à 25 témoins sains (âge moyen de 47 ans). On pense que l'expansion pathogène du C9ORF72 représente plus de 30 répétitions.
Les sujets de l'étude ont été scannés avec FDG-PET et IRM, et les scientifiques ont mesuré la chaîne légère (NfL) et la chaîne lourde du neurofilament; ces marqueurs de lésions neuronales sont apparus dans le LCR de 16 des 17 porteurs de mutation C9ORF72.
Les chercheurs ont constaté qu'il y avait significativement moins d'activité métabolique du glucose dans des zones discrètes du cerveau - en particulier dans le cortex insulaire et operculaire et les thalami - dans jusqu'à 82% des porteurs de mutation.
Ils ont également constaté une augmentation de l'absorption du traceur dans la région péri-rolandique chez 71% des porteurs de la mutation C9ORF72. Trois participants à l'étude avec l'expansion répétée avaient des niveaux élevés de NfL, mais les différences entre ceux avec la mutation et les contrôles sains n'étaient pas statistiquement significatives.
Le Dr Van Damme a déclaré qu'une élévation de la NfL chez quelques participants n'était pas une surprise, car d'autres études ont observé que la NfL augmentait généralement environ un à trois ans avant l'apparition des signes cliniques. Étant donné la pénétrance incomplète de C9ORF72, il n'est toujours pas clair quand et même si tous les participants développeront des symptômes cliniques de SLA ou de FTD.
Tous les porteurs de la mutation C9ORF72 ont subi un examen neurologique complet et le neurologue a trouvé de légers signes d'anomalies des motoneurones supérieurs chez 12 des 17 personnes atteintes de la mutation. "Comme la présence d'un signe de Hoffman ou d'un clonus de la cheville n'est pas nécessairement anormale chez les jeunes, nous n'avons considéré que la présence d'une secousse de la mâchoire, d'un signe de Babinski, d'une hyperréflexie et d'une augmentation du tonus musculaire pour de plus amples analyses", ont écrit les auteurs de l'étude.
Cinq des 17 porteurs de mutation C9ORF72 ont dévié de la norme sur la batterie cognitive - l'Édimbourg Cognitive and Behavioral ALS Screen. Le fonctionnement exécutif a été affecté chez trois porteurs de mutation (18%) et une autre personne a obtenu un faible score de fluidité verbale tandis qu'une autre a montré une altération du sous-domaine de la mémoire de l'outil de dépistage cognitif.
 « Aujourd'hui, des oligonucléotides antisens sont en essais cliniques avec des patients SLA porteurs de la mutation C9ORF72. Si tout va bien, si ces essais s'avèrent fructueux, nous pouvons commencer à penser à des études sur des porteurs asymptomatiques. » - DR. PHILIP VAN DAMME
« Aujourd'hui, des oligonucléotides antisens sont en essais cliniques avec des patients SLA porteurs de la mutation C9ORF72. Si tout va bien, si ces essais s'avèrent fructueux, nous pouvons commencer à penser à des études sur des porteurs asymptomatiques. » - DR. PHILIP VAN DAMME
Les résultats FDG-PET n'étaient pas seulement des changements de groupe, mais pouvaient être vus au niveau individuel, suggérant qu'ils pourraient être utilisés comme biomarqueurs pendant les stades précliniques de la maladie. Cela devient plus important, a déclaré le Dr Van Damme, lorsque des oligonucléotides antisens et d'autres thérapies géniques deviennent disponibles pour traiter des personnes des années avant le début des symptômes cliniques.
Il n'y avait pas d'association significative entre les résultats de la TEP et l'âge, les résultats du motoneurone supérieur, les résultats cognitifs ou les niveaux de neurofilament. L'IRM a révélé l'implication de régions similaires; cependant, les images de fréquence montraient que le FDG-PET semblait plus sensible. Les régions hypométaboliques sur les examens TEP trouvés dans les patients de l'étude asymptomatique sont similaires à celles trouvées sur les études d'imagerie chez les porteurs symptomatiques.
« Le schéma hypométabolique peut indiquer que la région est moins active ou qu'il y a atrophie, » a ajouté le Dr Van Damme. « Il était intéressant de noter que les changements de glucose cérébral n'étaient pas plus variables. »
Les scientifiques ont déclaré qu'une explication potentielle de la raison pour laquelle certaines zones des scanners TEP montraient un schéma hypermétabolique était que ce schéma pouvait représenter un mécanisme compensatoire ou une réponse à la neuroinflammation.
« Nous suivons environ 60 familles avec une mutation C9ORF72, » a déclaré le Dr Van Damme. « De nombreux membres de la famille souhaitaient des tests génétiques (et des conseils) pour voir s'ils étaient porteurs de la mutation. Les membres de ces familles sont très motivés à participer à la recherche. »
Les chercheurs continueront à étudier les familles avec ces mutations au fil du temps. «Il y a encore tant de questions sans réponse sur la maladie. Nous savons que la pénétrance de cette mutation n'est pas complète. J'ai vu un patient dans la quarantaine souffrant de la maladie et l'un des parents a porté la même mutation dans la quarantaine sans aucun signe clinique de maladie. Il sera intéressant de découvrir ce que nous voyons au fil du temps », a déclaré le Dr Van Damme.
« Aujourd'hui, des oligonucléotides antisens font l'objet d'essais cliniques avec des patients SLA porteurs de la mutation C9ORF72. Si tout va bien, si ces essais s'avèrent fructueux, nous pouvons commencer à penser à des études sur des porteurs asymptomatiques. »
Commentaire d'experts
« Pour les personnes vivant avec une mutation C9ORF72 (ou d'autres anomalies génétiques qui mèneront presque certainement à la FTD ou à la SLA si la personne vit assez longtemps), nous avons désespérément besoin d'imagerie et de biomarqueurs fluides détectables dans le cerveau qui nous indiquent quand les changements associés à la maladie commencent à se produire. », a déclaré Bradford Dickerson, MD, FAAN, directeur de l'unité des troubles frontotemporaux au Massachusetts General Hospital et professeur de neurologie à la Harvard Medical School.
« Les biomarqueurs comme l'hypométabolisme du glucose qui nous disent que le cerveau ne fonctionne pas normalement seront alors, espérons-le, utilisables pour mesurer si les traitements pourraient stabiliser ou améliorer la fonction cérébrale. Nous concevons maintenant des essais cliniques et avons besoin de plus de biomarqueurs comme celui-ci. »
William W. Seeley, MD, professeur de neurologie de la famille Zander, professeur de neurologie et de pathologie, et directeur de l'Université de Californie, San Francisco Neurodegenerative Disease Brain Bank au UCSF Memory and Aging Center, a ajouté: «La principale question soulevée par ces résultats, qui reproduisent et étendent les travaux antérieurs est: Quand ces anomalies apparaissent-elles? Il est tentant de supposer que les résultats représentent une neurodégénérescence naissante, mais un impact sur le développement de cette mutation à vie est également une possibilité. Si les changements sont le résultat d'un développement anormal, cela changerait notre façon de penser et de déployer des biomarqueurs d'imagerie dans des porteurs de gènes C9ORF72 présymptomatiques. Des études longitudinales et en début de vie sont nécessaires pour résoudre ce problème. »
Traduction : Christina Lambrecht
Source : Neurology Today


